Centre D’Investigation Clinique & Épidémiologique (CIEC)
Le CIEC soutient les institutions de recherche et de soins de santé, les universités internationales et les acteurs de l’industrie pharmaceutique, en leur fournissant des services et des recherches cliniques de haute qualité.
Missions
Le Centre d’Investigation et d’Epidémiologie Clinique (CIEC) jouit d’une réputation croissante dans le domaine de la recherche clinique. Agissant en tant que centre national coordonnant les activités de recherche clinique impliquant des médecins dans divers domaines médicaux, le CIEC est un interlocuteur pour les industries pharmaceutiques désireuses de mener des essais cliniques au Luxembourg. Le CIEC est synonyme d’excellence en matière de soutien opérationnel à la recherche clinique, tout en garantissant le respect des droits des patients et de la confidentialité des données et en offrant la possibilité d’accéder à de nouvelles approches thérapeutiques innovantes autrement inaccessibles.
Le CIEC soutient les institutions de recherche et de soins de santé, les universités internationales et les acteurs de l’industrie pharmaceutique, en leur fournissant des services et des recherches cliniques de haute qualité. Au cours des dix dernières années, le CIEC a coordonné plus de 7 000 participants à 140 projets de recherche et essais cliniques universitaires ou pharmaceutiques. Il vise également à mieux répondre aux besoins des patients et à améliorer leur qualité de vie en augmentant la recherche clinique pertinente et innovante au Luxembourg, y compris le développement de la recherche clinique et translationnelle.
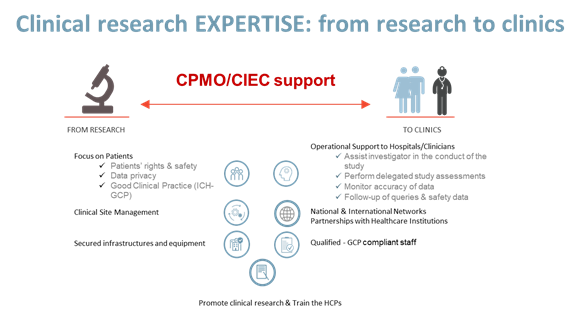
Fournir:
- Un soutien opérationnel et éducatif dans la mise en place de projets de recherche clinique pour les hôpitaux, les professionnels de la santé et les chercheurs, y compris des conseils en matière de réglementation et d’éthique
- Un accès à des approches/stratégies thérapeutiques nouvelles et innovantes pour les patients grâce à la participation à des études cliniques
- Un accès aux réseaux de recherche clinique (ECRIN, EFGCP, EUPATI…)
Protéger:
- Droits et sécurité des patients
- Confidentialité des données
- Bonnes pratiques cliniques (ICH-GCP) :
- En 10 ans : de 0 à 36 procédures, modèles et procédures opérationnelles standardisées.
- Audit des bonnes pratiques cliniques (BPC) réalisé en mars 2018
- Certifications BPC individuelles du personnel du CIEC (mise à jour annuelle)
- Certification ISO 9001
Promouvoir:
- • Communication et valorisation de la recherche clinique
- • Recherche clinique conformément aux Bonnes pratiques cliniques (ICH-GCP)
- • Intégrité et éthique de la recherche
Participer:
- Communication et valorisation de la recherche clinique
- Bonnes pratiques cliniques (ICH-GCP)
- Réseaux : ECRIN, EFGCP, etc.

Gantenbein
Partenaires
Projets et essais cliniques

Membres de l’équipe
Publications scientifiques
-
Publisher Correction – 02/09/2022
-
Age at onset as stratifier in idiopathic Parkinson’s disease – effect of ageing and polygenic risk score on clinical phenotypes – 09/08/2022
-
Interim analysis of COVID-19 vaccine effectiveness against Severe Acute Respiratory Infection due to laboratory-confirmed SARS-CoV-2 among individuals aged 30 years and older, ECDC multi-country study – second update – 14/03/2022
-
Exploring the association between patient characteristics and emergency department use in Luxembourg – 01/01/2022
-
An open-label randomized controlled trial of the effect of lopinavir/ritonavir, lopinavir/ritonavir plus IFN-β-1a and hydroxychloroquine in hospitalized patients with COVID-19 – 01/12/2021
-
Systematic review and network meta-analysis of the efficacy of existing treatments for patients with recurrent glioblastoma – 09/04/2021
-
Repurposed Antiviral Drugs for Covid-19 – Interim WHO Solidarity Trial Results – 11/02/2021
-
Association of diet quality indices with serum and metabolic biomarkers in participants of the ORISCAV-LUX-2 study – 01/01/2023
-
Associations Between Wearable-Specific Indicators of Physical Activity Behaviour and Insulin Sensitivity and Glycated Haemoglobin in the General Population – 12/12/2022
-
Publisher Correction – 02/09/2022
Actualités associées

Postes à pourvoir
Il n’y a pas d’offres d’emploi correspondant à cette page pour le moment. Vous pouvez consulter toutes les offres d’emploi en cliquant sur le bouton ci-dessous.